【研发】PD-1/L1不拼速度拼设计

PD-1/L1国内研发又有了令人瞩目的进展。
11月底,康宁杰瑞和思路迪宣布KN035重组人源化PD-L1 单域抗体Fc 融合蛋白注射液通过美国FDA审评,获准开展临床研究。据了解,这也是首个在美进入临床并且由中国企业自主开发和制造的抗体类创新药。
《医药经济报》记者梳理ClinicalTrials.gov网站上PD-1/L1领域的临床试验登记信息时发现,目前全球范围内至少有400个相关的临床试验正在进行,其中大陆地区数量约20余个。
涉及中国或中国企业的PD-1/L1抗体临床试验进展
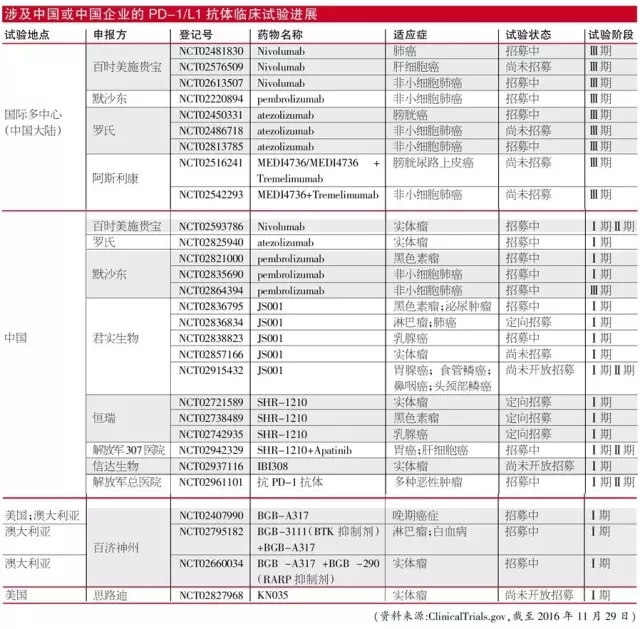
(点击图片可放大)
从国内市场来看,百时美、默沙东等跨国药企已经紧锣密鼓地布局了相关产品,本土企业君实生物、恒瑞医药、信达生物也率先进入Ⅰ期临床研究。由于不少项目仍处于早期研究阶段,未来还将有一大波PD-1/L1抗体进入临床试验。
[趋势] 适应症争夺战一触即发
目前国内PD-1/L1抗体Ⅰ期临床试验刚刚启动,在难与跨国药企比速度的情况下,临床试验设计的合理性对于本土药企而言将有所作为
据了解,PD-1/L1抗体已被FDA批准用于黑色素瘤、肺癌、膀胱癌等多种适应症。位于第一梯队的百时美施贵宝和默沙东已斩获数个适应症;罗氏、默克、辉瑞、阿斯利康紧随其后,在多种适应症中进一步挖掘PD-1/L1抗体的潜力。
记者注意到,尽管这些第一梯队开外的PD-1/L1抗体企业的临床试验项目中也出现了非小细胞肺癌或黑色素瘤适应症,但策略上已经产生了明显区分。比如利用自身产品管线的联合疗法数量远远多于单药疗法,侧重与传统一线化疗药物的对比。还有一大亮点,就是综合利用孤儿药地位、优先审评、快速通道以及突破性药物资格等多种渠道缩短审评审批周期。
目前国内PD-1/L1抗体Ⅰ期临床试验刚刚启动,虽然目前看似跨国药企和本土药企几乎站在同一起跑线上,但跨国药企按进口注册报批,速度应该是比国内企业快。从现有披露的信息来看,肺癌和黑色素瘤两大适应症很有可能成为众多企业争夺的焦点。
事实上,除了肺癌,胃癌、肝癌、食管癌在中国发病率和死亡率也相对较高,由于这些癌种在西方国家整体发病率并不高,一直没有引起跨国药企足够的重视。相当多医疗领域专家也在不同场合频繁呼吁企业关注中国特有的高发病率癌种,有针对性地进行药物研发。
“有数据显示,在肝癌中PD-1抗体比索拉非尼相对优效。”康宁杰瑞董事长徐霆在采访中表示,考虑到中国肝癌领域存在未被满足的需求,在接下来的临床试验中将首先从肝癌这一适应症入手,争取以此为突破口寻求尽早上市的机会,在取得疗效的同时可能再逐步拓展至肺癌等其他适应症。
随着PD-1/L1抗体陆续进入临床试验,一个合理的临床试验设计的价值将愈发凸显。一位从事创新药研发的专家曾告诉记者药物临床失败不一定是药物本身不好,也有可能与临床设计时的指标设置有关联,比如Opdivo一线治疗非小细胞肺癌Ⅲ期研究失败就是前车之鉴。
不过,该专家指出,国内在创新药临床试验方面的经验并不丰富,中国很少有医生专门从事新药临床试验,尤其对机理全新的创新药缺乏经验,而这类药物的成功往往离不开高技术含量的临床试验设计。此外,真正具有药物开发经验的临床人才也属于稀缺资源。对于涉足PD-1/L1领域的企业而言,这些无疑是即将到来的挑战。
[难题] 什么才是核心竞争力?
未来不可避免迎来多个品种上市,因此必须全方位寻找不可取代的优势(区分度),挖掘未被开发的空间
记者曾就国内PD-1/L1市场空间是否饱和请教过多位业内专家,但得到的意见截然相反。
“肯定者”认为,先进入的企业站稳脚跟后,一定会通过扩大适应症占有市场,挤压后来企业的生存空间,况且最终能有几家企业能盈利还充满不确定性。
“否定者”认为,中国肿瘤患者数量不断攀升,具有广谱抗癌潜力的PD-1/L1抗体也会随之扩大市场,这么多家企业涌进去也足以养活。
不过,专家们在差异化竞争上形成了一致看法——目前国内PD-1/L1领域的竞争非常激烈,未来将不可避免地迎来多个品种上市,企业一定要在某个方面形成不可取代的优势才有可能在市场中脱颖而出。
“无论是商业模式、给药途径还是诊断方式,乃至最简单的储存方式,企业都要思考如何形成区分度。”徐霆告诉记者,康宁杰瑞在研发PD-L1抗体的过程中从三个维度上打造了区分度:首先,结构上采用的是具有较强的亲和力和穿透性的单域抗体;其次,给药方式采用的是皮下注射,提高了医患使用的便利性;“此外,我们通过与思路迪的合作引入了精准医学的概念,希望在病人筛选、预后等方面取得突破性进展。”
当被问及PD-1/L1抗体大战中企业制胜的关键因素如何排序时,徐霆给出了自己的答案:成本、成药性、产品独特性、伴随诊断、与自身产品线的组合、下一步的拓展开发、销售渠道。
据公开资料显示,目前已上市的PD-1/L1抗体药物价格约100万元人民币/年。有专家直言,即使这些药物立刻引入国内,也会面临“有疗效没市场”的困境。另一方面,本土企业可以通过生产工艺开发等多种手段将现有价格降至一半甚至三分之一,再利用招标采购等资源形成后发优势,“更多的病人能够负担得起,市场才能真正大起来。”
另外,PD-1/L1抗体在分子水平和基因水平还有很多机理尚未阐明,如果国内企业能够苦下功夫研究,或许能够开辟出新的市场空间。“肿瘤的发生发展是一个动态的过程,肿瘤微环境也会随着治疗进展不断发生变化。”徐霆指出,如何监测这种变化是长期以来肿瘤治疗的难关之一,“未来我们将通过同位素标记和PET-CT在临床试验期间对肿瘤标志物进行动态监测,判断其与疗效的相关性,推进品种上市,并同步开发与药物配套的伴随诊断。”徐霆还指出,下一步基于PD-1/L1抗体的组合疗法会进入主流,关于组合的选取以及如何组合等方面,还有大量前期工作要做。
记者通过采访了解到,受到时间、空间等条件制约,目前抗PD-L1的免疫组化(IHC)检测非常有限,业内对于疗效与诊断是否相关以及相关程度上一直存在争议。例如:PD-L1标志物来源于免疫系统还是肿瘤表面哪个更合理?除了PD-L1是否还存在其他标志物?部分PD-L1表达阴性的患者为何也出现了响应?这些质疑都需要经过大量实际检验和数据统计确认。
“尽管现在有多个PD-1/L1抗体药物已经或即将上市,但是细究起来仍然有很多未知的空间。可以说,肿瘤免疫治疗从PD-1/L1抗体开始才刚起步,我们还有五年、十年甚至更长的时间去探索。”徐霆说道。
文章来源:医药经济报

