又有八个过亿注射剂申报再评价,孟鲁司特钠颗粒首仿获批

来源:米内网原创
总体承办情况
据MED中国药品审评数据库2.0统计,2018年7月CDE共承办药品注册申请731个,总体同比继续上升,除进口申请和6月基本持平外,新药申请和仿制申请均有所回落。
图1:2018年1-7月CDE承办药品注册申请情况(按受理号计)
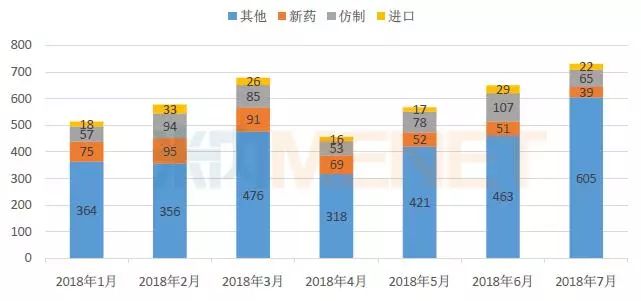
(数据来源:MED中国药品审评数据库2.0,下同)
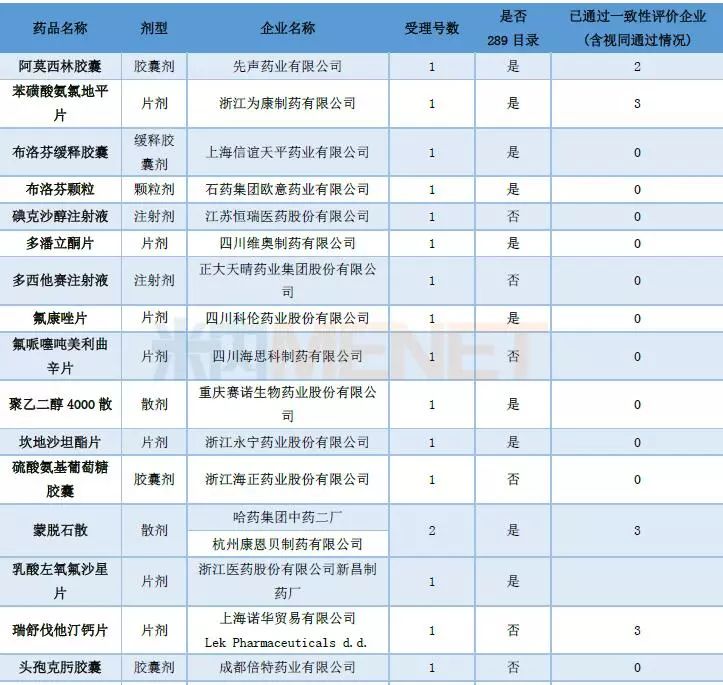
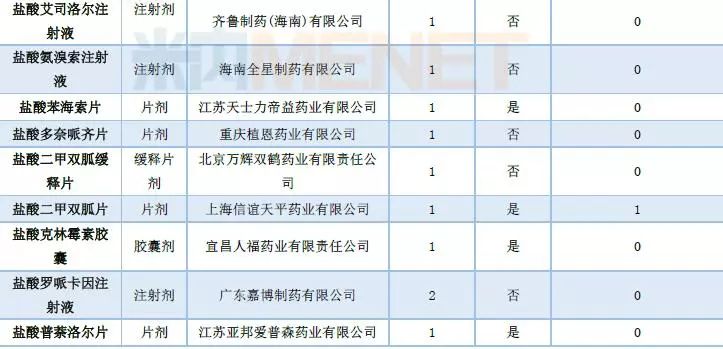
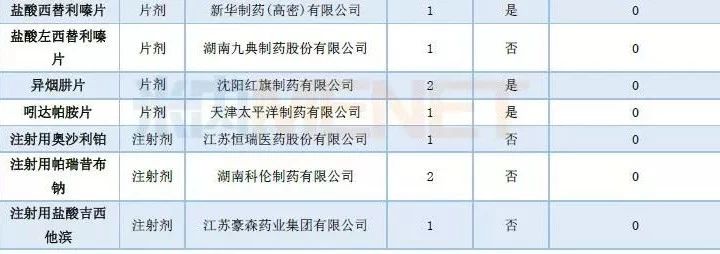
7月有36个仿制药再评价申请进入CDE,涉及32个品种(6月有36个品种),其中注射剂有8个,口服制剂有24个,据米内网中国城市公立医院化学药终端竞争格局显示,8个注射剂2017年销售规模均过亿,其中盐酸氨溴索注射液达65亿元。
苯磺酸氨氯地平片、蒙脱石散、瑞舒伐他汀钙片目前均有3家企业通过一致性评价,阿莫西林胶囊有2家,而盐酸二甲双胍片有1家。
恒瑞医药和上海信宜天平药业均提交了两个品种的再评价申请,其中恒瑞医药的两个品种均为注射剂,目前恒瑞医药再评价在审品种达12个。湖南科伦制药提交其首仿产品注射用帕瑞昔布钠一致性评价申请。
表1:2018年7月CDE仿制药再评价申请承办情况
国内1类新药承办:豪森药业甲磺酸氟马替尼片申请上市
7月CDE共承办国内新药申请39个,其中属于1类新药的申请有27个,涉及14个品种。
江苏豪森药业1类新药甲磺酸氟马替尼片申请上市,拟用于治疗慢性粒性细胞性白血病。
珍宝岛药业旗下子公司哈尔滨珍宝制药提交HZB0071原料及片剂的临床申请,HZB0071是一款ATK抑制剂,用于抗肿瘤治疗,同时也是珍宝岛药业首个创新药。此外,北京艺妙医疗科技以及广州百暨基因科技各提交一款CAR-T疗法药物的临床申请。
表2:2018年7月国内1类新药承办情况
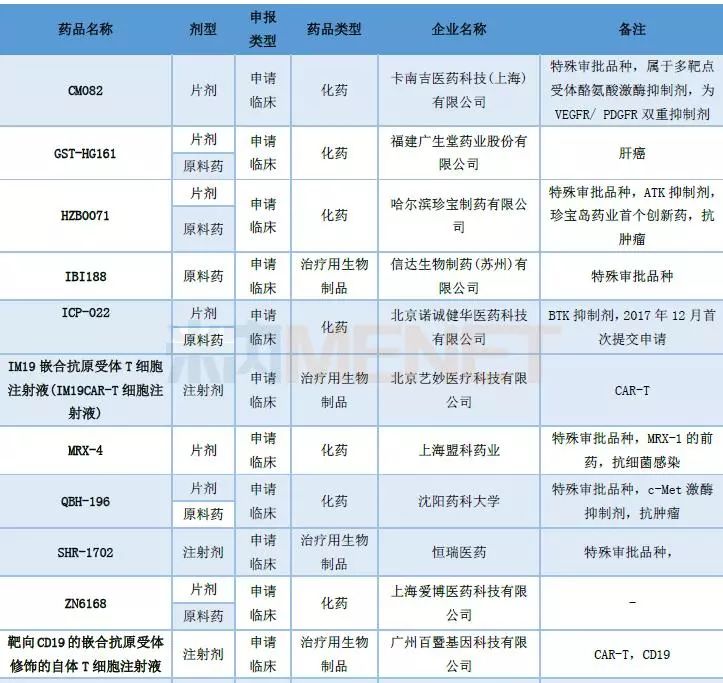

国内仿制药承办:他达拉非片在审企业达11家
7月CDE共承办仿制申请65个,涉及46个品种,其中有14个品种目前为国内独家品种。
奥氮平片、注射用培美曲塞二钠、甲磺酸伊马替尼片目前均有1家企业通过仿制药一致性评价,而瑞舒伐他汀钙片则有3家。
广东东阳光药业在7月仿制申请最多,共有4个品种,分别是奥氮平口崩片、利格列汀二甲双胍片、利格列汀片以及他达拉非片。据米内网数据,他达拉非片在国内是礼来的独家品种,目前在审仿制申请有23个(按新注册分类计),涉及11家企业,竞争十分激烈。
表3:2018年7月仿制申请承办情况
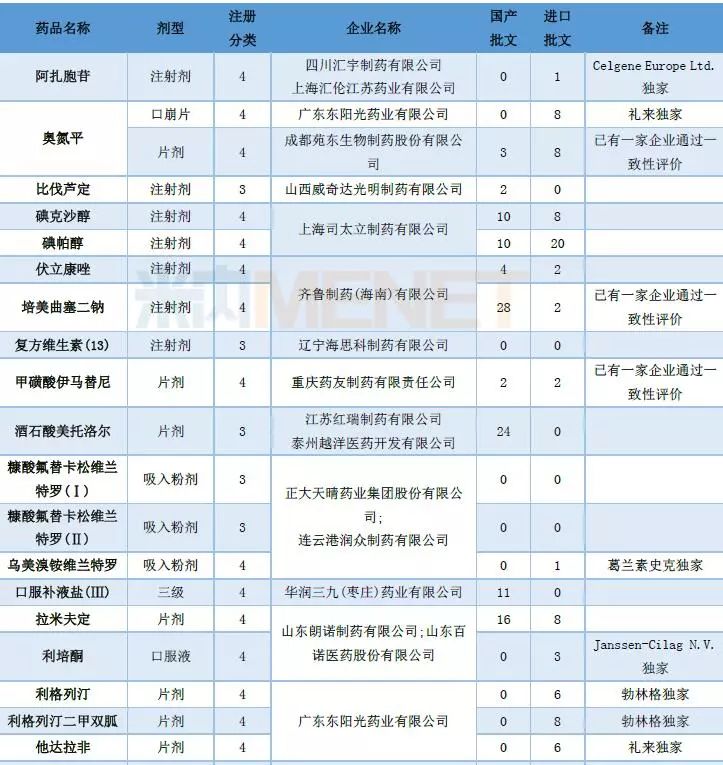
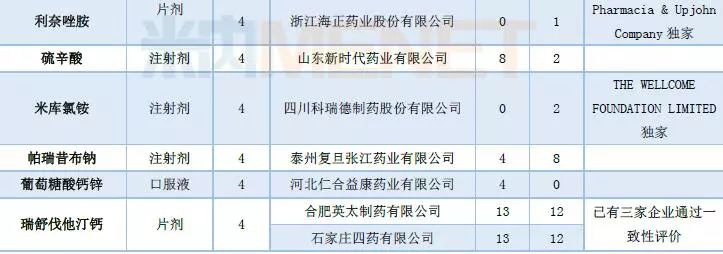
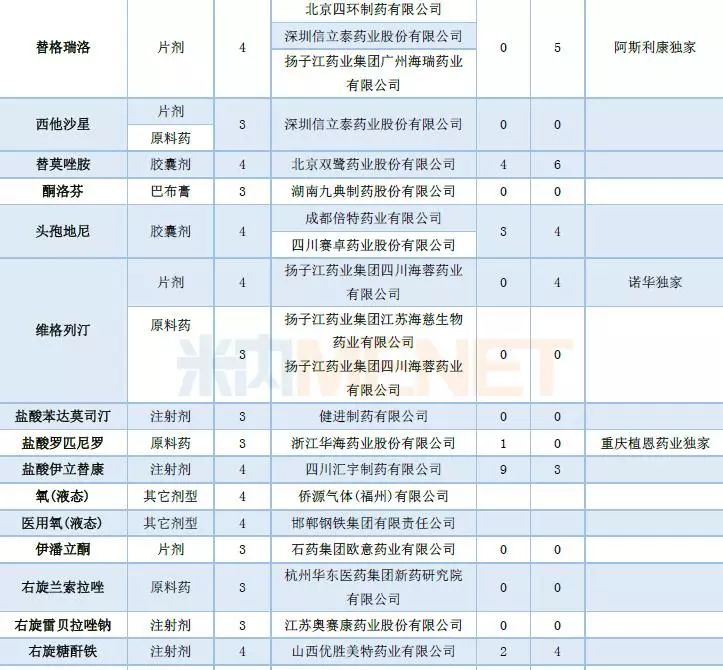

进口申请承办:有3个品种为首次承办品种
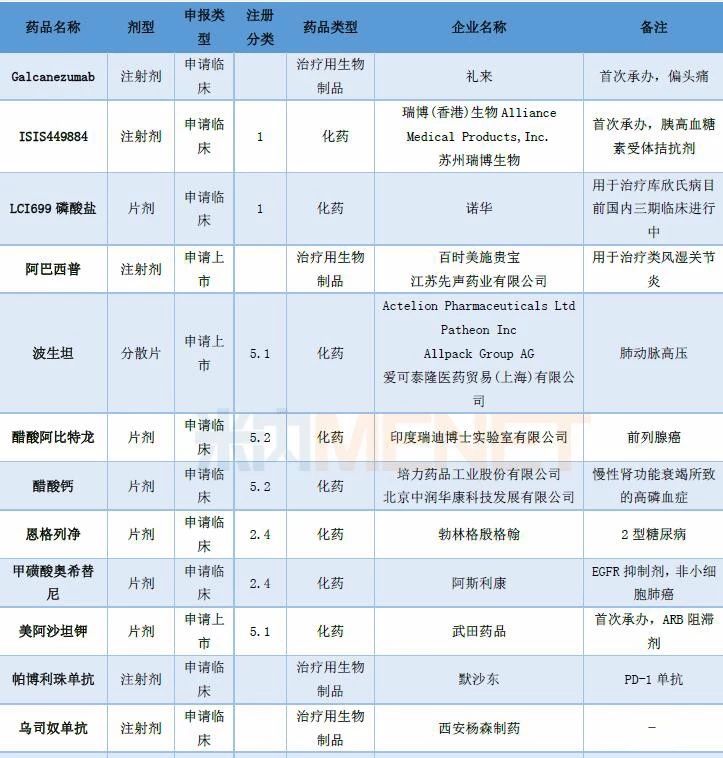
7月CDE共承办进口申请22个,涉及14个品种。阿巴西普、波生坦分散片、美阿沙坦钾片申请上市。Galcanezumab注射液、ISIS449884注射液、美阿沙坦钾片为CDE首次承办品种。
表4:2018年7月CDE进口申请承办情况

获批情况:孟鲁司特钠颗粒首仿获批
国家药品监督管理局在7月发布了第五批已批准通过仿制药质量和疗效一致性评价品种目录,本批有16个品规通过仿制药质量和疗效一致性评价,同时本批也是国家药监局集中公布的最后一批,此后通过一致性评价的品种将直接收录到《中国上市药品目录集》,不再分批公告。
华润赛科药业的苯磺酸氨氯地平片通过一致性评价,华润赛科药业成为第三家苯磺酸氨氯地平片一致性评价的企业。齐鲁制药盐酸特比萘芬片通过一致性评价,齐鲁制药是首家通过盐酸特比萘芬片一致性评价的企业。
石药集团盐酸二甲双胍片出口制剂转报国内获批,视同通过一致性评价。杭州民生滨江和上海安必生制药联合申报的4类仿制药孟鲁司特钠片及咀嚼片获批,视同通过一致性评价,其中咀嚼片剂型也是出口制剂转报国内。
长春海悦药业的孟鲁司特钠颗粒也在7月获批上市,是国内孟鲁司特钠颗粒的首仿产品,此前以“儿童用药”被纳入优先审评品种。据了解,长春海悦药业的孟鲁司特钠颗粒目前已完成BE试验,预计之后能快速通过一致性评价。
据米内网中国公立医疗机构终端竞争格局显示,孟鲁司特在2017年的市场规模超过23亿元,总体市场规模逐年上升。目前国内除默沙东的原研品外(69.72%),还有大冢制药(16.8%)和鲁南贝特制药(13.48%)的仿制品种,随着前述孟鲁司特品牌陆续上升,市场竞争将进一步加剧。
表5:2018年7月部分获批上市情况
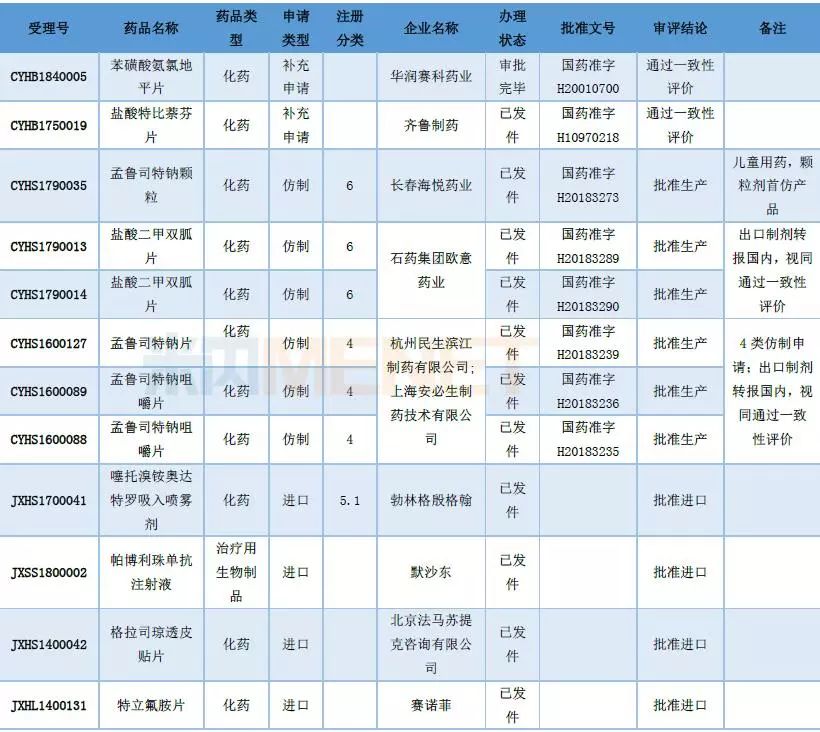
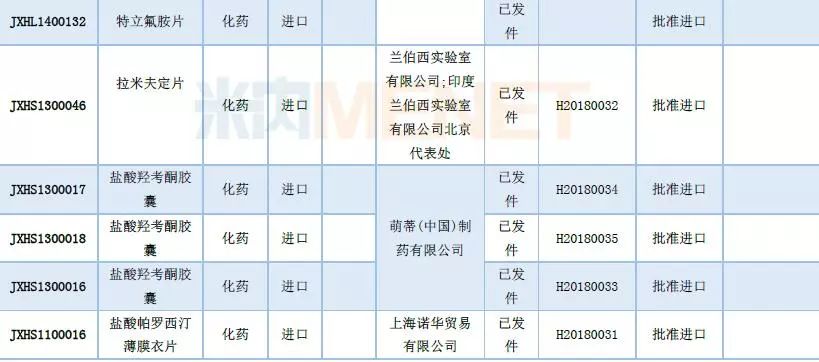
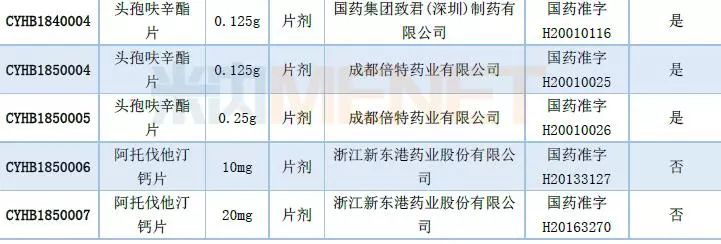
表6:第五批通过仿制药一致性评价品种
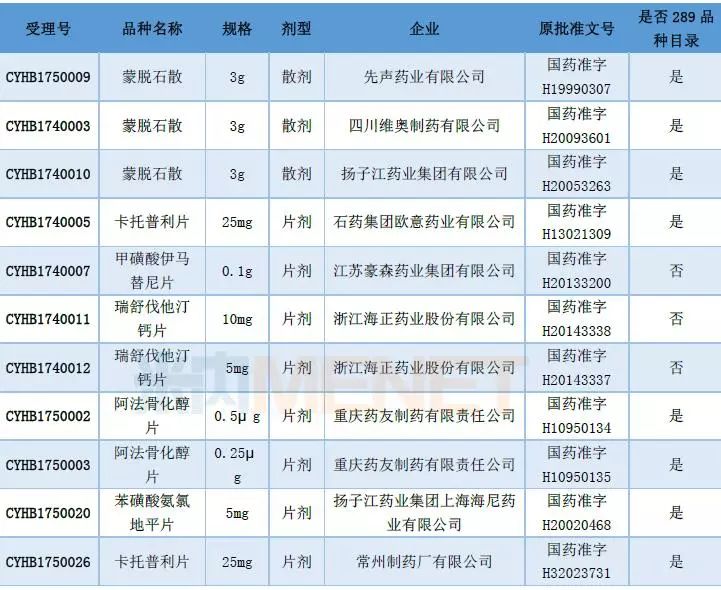
数据来源:米内网MED中国药品审评数据库2.0
声明:本网站部分文章和信息来源于互联网或原创作者/平台授权转载,不代表本订阅号赞同其观点和对其真实性负责,如有侵权请和我们联系处理,但若转载请务必注明原出处和作者。本平台刊载的各类文章重在分享,尊重原创,如有侵权请联系我们(010-67884870),我们将会在24小时之内删除。

